ısı ve sıcaklık farkları konu anlatımı

Isı ve sıcaklık farklı kavramlardır. Sıcaklık, bir sistemde rastgele hareket eden moleküllerin ortalama kinetik enerjisinin bir göstergesidir.
Maddenin molekül veya atomlarının ortalama kinetik enerjisi artarsa sıcaklığı da artar. Sıcaklık, skaler bir büyüklüktür, termometre ile ölçülür.
ISI birim sisteminde sıcaklık birimi Kelvin’dir ancak günlük yaşantıda çoğunlukla Celcius derece (˚C )kullanılır.
Maddeden maddeye veya aynı maddenin bölgeleri arasında aktarılan enerjiye ısı denir. Maddeye enerji aktarıldığında maddenin ortalama kinetik enerjisinin artmasına yani sıcaklığının artmasına neden olur.
Isı skaler bir büyüklüktür. Birimi joule’dür. Isı enerjisini direk olarak bir aletle ölçemeyiz ancak kalorimetre kabı yardımıyla hesaplayabiliriz.
Çevremizde bazen rastladığımız; “vücut ısısı”, “suyun ısısı”, “havanın ısısı” kullanımları yanlıştır. Doğru kullanım “vücut sıcaklığı”, “suyun sıcaklığı”, “havanın sıcaklığı” şeklinde olmalıdır.
İç Enerji
Maddenin atom veya moleküllerinin hareketinden kaynaklanan kinetik enerjisi ile kimyasal bağlardan kaynaklanan potansiyel enerjisinin toplamına iç enerji denir.
İç enerji türetilmiş ve skaler bir büyüklüktür. Birimi joule’dür. İç enerji maddenin miktarına, cinsine ve sıcaklığına bağlıdır.
Maddeye dışardan enerji verildiğinde atom veya moleküllerin kinetik enerjisi artar, maddede iç enerji olarak depolanır sonuç olarak sıcaklığı artar. Eğer madde dışarıya enerji veriyorsa iç enerjisi azalır dolayısıyla sıcaklığı azalır.
Termometre Çeşitleri
Termometreler, maddenin sıcaklık karşısında değişikliğe uğramasından (genleşmesinden) yararlanılarak yapılmıştır. Kullanılacağı sıcaklık aralığına uygun olan madde seçilerek farklı termometreler yapılmıştır.
Sıvılı termometreler, gazlı termometreler, metal termometreler olmak üzere farklı termometreler vardır.
1- Sıvılı Termometreler
Sıvılı termometreler, kullanılan sıvının donma ve kaynama sıcaklıkları arasındaki sıcaklıkları ölçebilir. Sıcaklık artınca genleşen sıvı boruda yükselir böylece sıcaklığı ölçmüş oluruz.
Sıcaklığın düşük olduğu yerlerde alkollü termometre kullanılır.
Sıvılı termometrelerin hassasiyeti (duyarlılığı);kullanılan kılcal borunun kalınlığına (kesitine), kılcal borunu cinsine, içindeki sıvının cinsine, haznenin büyüklüğüne, bölme sayısına bağlı olarak değişir.
2- Gazlı Termometreler
Düşük sıcaklıklarda daha hassas ölçüm yapmak için gazlı termometreler kullanılır.
3- Metal termometreler
Yüksek sıcaklıklarda, fabrikalarda ve fırınlarda sıcaklık ölçmek için metal termometreler kullanılır.
4- Pirometre
Sıcaklığın yaklaşılmayacak kadar yüksek olduğu veya temas edilmeden ölçüm yapmak istediğimiz durumlarda kullanılan termometredir.
Sıcaklık Ölçeklendirmesi
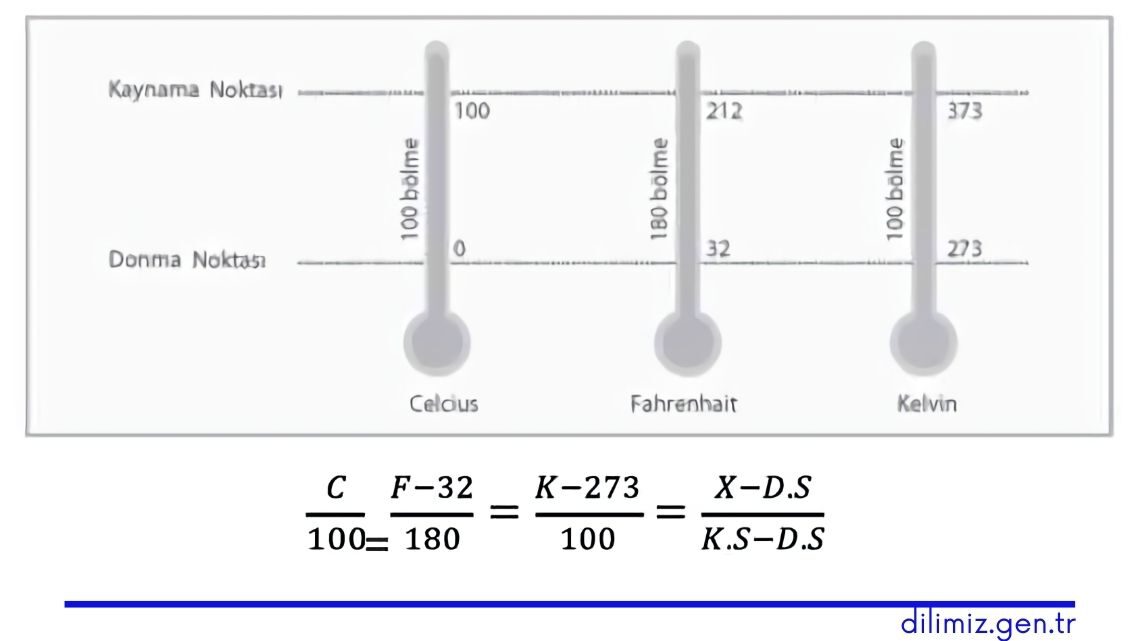
Öz Isı ve Isı sığası
Saf bir maddenin 1 gramının sıcaklığını 1˚C artırmak için gerekli ısı miktarına öz ısısı denir. Öz ısı “c” ile gösterilir birimi joule/kg veya cal/g ˚C ve maddeler için ayırt edici bir özelliktir. Öz ısı ile ilgili olarak;
- Öz ısı saf maddeler için ayırt edici bir özelliktir.
- Öz ısı madde miktarına bağlı olarak değişmez.
- Eşit miktarda farklı cins maddelere, eşit miktarda ısı verildiğinde öz ısısı az olan sıvının sıcaklığı daha fazla artar.
- Eşit miktarda farklı cins maddelerin çevreye verdikleri ısı, öz ısısı fazla olanın daha fazladır.
- Denizlerin karalardan daha geç ısınıp soğumasının nedeni suyun öz ısısı diğer maddelere göre fazla olmasıdır.
Bir maddenin sıcaklığını 1 ˚C artımak için gerekli ısı miktarına ısı sığası veya ısı kapasitesi denir C ile gösterilir . Matematiksel olarak;
Isı sığası= Kütle. Öz ısı C= m.c şeklinde ifade edilir.
Bknz: Öz ısı ve ısı sığası konu anlatımı
Isı alan ve Isı Veren Maddelerde Sıcaklık Değişimi
Maddenin sıcaklığındaki değişim maddenin aldığı ya da kaybettiği ısı miktarına, maddenin kütlesine ve öz ısısına bağlıdır.
Q, alınan veya verilen ısı; m, maddenin kütlesi; Δt, sıcaklık değişimi; c, öz ısı olmak üzere ısı alan ve ısı veren maddelerde sıcaklık değişimi;
ΔT = Q / m.c olarak ifade edilir.
Hâl Değişimi
1- Erime ve Donma
Her maddenin erime sıcaklığı farklıdır. Katı hâldeki maddenin enerji alarak sıvı hâle geçmesine erime denir. Madde erirken sıcaklığı artmaz, erime bitene kadar sabit kalır.
Madde erirken maddeye verilen enerji hâl değişiminde kullanılır. Sıvı hâldeki maddenin enerji kaybederek katı hâle geçmesine donma denir.
2- Yoğuşma ve Buharlaşma
Sıvı yüzeyindeki moleküller kinetik enerjilerini yeterince artırdığında gaz hâline geçer bu olaya buharlaşma denir. Buharlaşma her sıcaklıkta olur.
Gaz hâldeki moleküllerin sahip olduğu enerjiyi kaybederek gaz hâlden sıvı hâle geçmesine yoğuşma denir.
Sıvı moleküllerinin enerji vermeye devam edildiğinde hızlarının çok arttığını kabarcıklar oluşturarak sıvı yüzeyinden ayrıldığı gözlenir bu olaya kaynama denir. Kaynama buharlaşmanın özel bir durumudur.
3- Süblimleşme ve Kırağılaşma
Naftalin, kuru buz (katı karbondioksit) gibi bazı maddelerin doğrudan katı hâlden gaz hâle geçmesine süblimleşme denir.
Maddenin gaz hâlden doğrudan sıvı hâle geçmesine ise kırağılaşma (kristalleşme) denir. Aşağıda hâl değişimleri bir şema üzerinde gösterilmiştir.
4- İyonizasyon ve Deiyonizasyon
Gaz hâlindeki maddenin ısı alarak plazma hâline geçmesi olayına iyonizasyon denir. Plazma bir maddenin ısı kaybederek gaz hâline geçmesi olayına deiyonizasyon denir.
Hâl Değiştirme Isısı
Erime sıcaklığına ulaşmış katı bir maddenin 1 gramının sıvı hâle gelmesi için gerekli enerji miktarına “erime ısısı” denir.
Donma sıcaklığında bulunan 1gram sıvı maddenin katı hâle geçmesi için verdiği enerji miktarına “donma ısısı” denir.
Aynı madde için donma ve erime ısıları birbirine eşittir. Birimi cal/g’dır.
Q: Madde hâl değiştirirken gerekli olan enerji miktarı m: Hâl değiştiren maddenin kütlesi L: Erime ısı olmak üzere ısı miktarı Q= m.L olarak ifade edilir.
Isıl Denge
Sıcaklıkları farklı maddelerin aralarındaki ısı akışı, maddelerin sıcaklıkları eşitlenince durur. Bu sıcaklığa denge sıcaklığı denir. Denge sıcaklığı Td ile gösterilir.
Denge sıcaklığında olan maddeler ısıl (termal) dengedeki maddeler adı verilir. Isıl dengedeki maddelerin sıcaklıkları eşittir. Maddelerin denge sıcaklığı, sıcaklığı büyük olan maddeninkinden daha büyük; sıcaklığı küçük olanından küçük olamaz.
Dış ortamdan izole edilmiş ve birbirine temas eden iki maddenin arasındaki ısı alışverişinde maddeler ısıl dengeye ulaştığında birinin verdiği ısı miktarı diğerinin aldığı ısı miktarına eşittir. Bu durumu matematiksel olarak; Qalınan=Qverilen
Enerji İletim Yolları ve Enerji İletim Hızı
Enerji İletim Yolları
Isının İletim Yoluyla Yayılması
Katı maddelerin atom veya moleküllerinin enerjilerini birbirlerine aktarmasına ısının iletim yoluyla yayılması denir. Isının iletim yoluyla yayılması için mutlaka ortama ihtiyaç vardır.
Isının Konveksiyon Yoluyla Yayılması
Maddenin sıcaklığının yüksek olduğu yerde yoğunluğu daha azalır, sıvı ve gaz maddelerde bu yoğunluk farkı olur.
Sıvı ve gaz maddelerde bu yoğunluk farkından dolayı atom ve moleküller yer değiştirirler bu sayede enerji madde içinde taşınmasına ısının konveksiyon yoluyla yayılması denir.
Isının konveksiyon yoluyla yayılması için mutlaka madesel ortama ihtiyaç vardır. Sobanın odayı ısıtması ve tenceredeki suyun kaynaması ısının konveksiyon yoluyla yayılmasına örnek verilebilir.
Isının Işıma Yoluyla Yayılması
Dünyamızın en önemli enerji kaynağı olan Güneş bize enerjisini ışıma yoluyla iletmektedir. Isının maddesel ortama ihtiyaç duymadan yayılmasına ısının ışıma yoluyla yayılması denir.
Katı Maddelerdeki Enerji İletim Hızı
Farklı maddelerin enerji iletim hızları farklıdır. Metallerin enerji aktarım hızları diğer maddelere göre daha fazladır. Metallerin enerji aktarım hızları serbest elektron sayılarına bağlı olarak değişiklik gösterir.
Maddelerin ısı iletkenliğini ısı iletim katsayısı ile ifade edilir.1 m2’lik yüzey alanına sahip maddelerin iki yüzeyi arasındaki sıcaklık farkından dolayı bir yüzeyinden diğer yüzeyine en kısa mesafede birim zamanda geçen ısı miktarına ısı iletkenlik katsayısı denir.
Birimi watt/metre. kelvin’dir. Isı iletkenlik katsayısı maddeler için ayırdedici bir özelliktir. Maddelerin ısı iletim hızı;
- Maddenin cinsine,
- Maddenin iki ucu arasındaki sıcaklık farkına,
- Maddenin kalınlığına,
- Enerji iletiminin gerçekleştiği maddenin yüzey alanına bağlıdır.
Enerji Tasarrufu
Ülkemizde de enerji tasarrufu sağlamak için binalarda ısı yalıtımı zorunlu hâle getirilmiştir. Enerji iletim hızı düşük olan maddelere yalıtım malzemeleri denir.
Binanın yalıtım malzemeleriyle kaplanarak yapılan enerji yalıtım işlemlerine “mantolama” adı verilir.
Binalar yapılırken tuğlaların kalın kullanılması veya kullanılan ince tuğlaların arasına strafor veya cam elyaf adı verilen maddeler konularak yapılması birer yalıtım örneğidir. Binalarda ısı yalıtımı sayesinde büyük oranlarda enerji tasarrufu sağlanmaktadır.
Hissedilen Sıcaklık Ne Demektir?
Hissedilen Sıcaklık, termometrenin ölçtüğü hava sıcaklığından farklı olarak, insan vücudunun hissettiği, algıladığı sıcaklıktır.
Bu sıcaklık, iklimsel çevre, giysilerin ısı direnci, vücut yapısı ve hareketlilik durumundan olduğu kadar, nem, rüzgâr meteorolojik faktörden etkilenir. Dolayısı ile sıcaklığı algılama ve hissetme kişiden kişiye değişiklik gösterir.
Küresel Isınma
Güneş ışınlarının atmosferdeki gazlar tarafından tutularak Dünya’nın sıcaklığının artması olayına sera etkisi adı verilir. Atmosfere salınan gazların sera etkisinin artırarak Dünya’nın ortalama sıcaklığının yükselmesine neden olmasına küresel ısınma denir.
Küresel ısınma iklim değişikliği, buzulların erimesi, deniz seviyesinin yükselmesi, bazı canlıların türlerinin ve tatlı su kaynaklarının azalması gibi durumlara yol açabilir.
Buzulların erimesi ile oluşan kara parçaları güneş enerjisini daha çok soğuracağı için dünyamızın sıcaklığının giderek artacağı tahmin edilmektedir.
Küresel Isınmaya Karşı Alınabilecek Tedbirler
- Yenilenebilir enerji kaynaklarını tercih etmek.
- Binalarda ısı yalıtımı sağlamak.
- Aydınlatmada verimli tasarruf ampülleri kullanmak.
- Toplu taşıma araçlarını kullanmak.
- Evsel atıkları geri dönüşümle tekrar kullanmak.
- Elektrikli eşyaları kullanmadığımız zaman tamamen kapatmak.
- Taşıtların hava ve yakıt filtrelerini zamanında değiştirmek.
- Su kullanımda tasarruflu olmak.
- Karbondioksit emilimini artırmak için ağaç dikmek.
Genleşme
Katı Ve Sıvılarda Genleşme ve Büzülme
Maddelerin enerji alışverişi sırasında sıcaklıklarının değişmesi sonucunda hacimlerinde meydana gelen değişikliğe “genleşme” denir.
Elektrik kablolarının kışın gergin olması yazın ise sarkması, demiryollarında rayların arasında veya köprülerde bırakılan boşluklar bırakılması genleşme ile ilgilidir.
Maddelerin genleşme miktarı atom ve moleküller arasındaki bağlara ve yapısına göre maddeden maddeye farklılık gösterir. Maddenin hacminde meydana gelen değişiklikle birlikte hacminin değişmesi olayının genel adı genleşmedir ancak maddenin sıcaklığının azalması sonucu hacminin küçülmesi olayına özel olarak “büzülme” adı verilir.
Sıcaklığı ayarlanan elektrikli aletin sıcaklığını belli bir değerde tutmak için termostat adı verilen düzenek kullanılır. Termostat, maddelerin aynı sıcaklık karşısında farklı miktarlarda genleşmesinden yararlanılarak iki farklı maddenin bir araya getirilmesiyle oluşmuş bir metal çiftidir.
Elektrik devrelerinde devreyi açıp kapatarak anahtar görevi görür. Termometre çeşitlerinden biri olan sıvılı termometreler, sıcaklığı değişen sıvının genleşmesi sonucu ölçüm yapar.
Genleşme olayında su diğer sıvılardan farklılık gösterir. Bu farklılık suyun donarken de genleşmesidir.
Hemen hemen tüm maddelerin katı hâldeki öz kütlesi sıvı hâldeki öz kütlesinden daha büyüktür fakat suyun öz kütlesi en büyük değerini (1g/cm³) +4˚C de yani sıvı iken alır çünkü +4˚C de su hacim olarak en küçük değere ulaşır. Soğutulan suyun hacmi 4˚C’ye kadar beklendiği gibi azalırken, 4˚C’den sonra artmaya başar.
Soğumayla beraber hacimdeki bu artış donma sırasında da devam eder. Tamamen su dolu bir şişeyi veya bardağı buzluğa koyduğumuzda şişenin veya bardağın çatlaması da suyun donarken hacminin artması nedeniyle olur.
Su buz hâline geçtiğinde belli bir hacme ulaşır dolayısıyla buzun öz kütlesi suyun öz kütlesinden daha küçük olduğu için buz suyun üzerinde yüzer. Suyun bu özel durumu sayesinde göllerin, denizlerin üst kısmı donarken su altındaki canlılar yaşamını sürdürebilmektedir.
Gaz molekülleri arasındaki uzaklık katı ve sıvı molekülleri arasındaki uzaklıktan daha fazladır.
Gaz moleküllerine enerji verildiğinde kinetik enerjileri ile birlikte moleküller arsındaki uzaklık daha da artacağı için gazlar da genleşir. Sıcak hava balonların ve dilek fenerlerinin havada yükselmeleri gazların genleşmesi ile ilgilidir.
Sıcaklık artışına bağlı olarak gazların genleşmesi sayesinde havaya yükselmektedir.